
APRNEWS: Révolution médicale – Découvrez le microrobot révolutionnaire de l’ETH pour une délivrance ciblée de médicaments
Des chercheurs de l'ETH ont mis au point un microrobot capable de transporter des médicaments de manière ciblée à des endroits précis du corps et qui a le potentiel d'être bientôt utilisé dans les hôpitaux.
Douze millions de personnes dans le monde sont victimes d’un accident vasculaire cérébral chaque année – beaucoup en meurent ou restent handicapées. Pour dissoudre le thrombus qui obstrue le vaisseau sanguin, on administre aujourd’hui des médicaments qui se répartissent dans tout le corps. Pour que la quantité nécessaire de médicament atteigne le thrombus, une dose élevée doit être administrée. Cela peut entraîner des effets secondaires importants, comme des hémorragies internes. Comme les médicaments ne sont souvent utilisés qu’à un endroit précis du corps, la recherche médicale tente depuis longtemps d’amener les produits pharmaceutiques là où ils doivent agir : Dans le cas d’un accident vasculaire cérébral, directement à proximité du thrombus. Une équipe de chercheurs de l’ETH a réussi des percées décisives à plusieurs niveaux, qu’elle présente dans la revue spécialisée page externeScience publient.
Des nanoparticules parfaitement adaptées sont nécessaires
Les chercheurs utilisent comme microrobot une capsule ronde qu’ils ont développée, constituée d’une enveloppe de gel soluble, qu’ils peuvent diriger magnétiquement à travers le corps et ainsi amener à destination. Dans la capsule, des nanoparticules d’oxyde de fer assurent les propriétés magnétiques. « Comme les vaisseaux du cerveau humain sont si petits, la capsule ne peut avoir qu’une taille déterminée. Le défi technique est qu’une capsule aussi petite ait des propriétés magnétiques suffisamment fortes », explique Fabian Landers, premier auteur de l’article et post-doctorant au Multi-Scale Robotics Lab de l’ETH Zurich.

Animation erklärt,wie der neue ETH-Mikroroboter funktioniert. (Video: ETH Zürich)
Pour que les médecins puissent suivre, grâce à l’imagerie par rayons X, la manière dont les patients sont traités.
se déplace dans les vaisseaux, il faut en outre un
agent de contraste. Pour ce faire, les chercheurs ont utilisé les techniques souvent utilisées en médecine.
Les nanoparticules de tantale utilisées dans ce cas sont plus difficiles à fabriquer.
sont plus lourds que les autres. Fonctionnalité magnétique »,
une visibilité par imagerie et un contrôle précis en un seul et même endroit.
microbots, nécessite une interaction parfaite entre les
Science et ingénierie des matériaux et robotique. Il nous a fallu de nombreuses années,
atteindre cet objectif », explique Bradley Nelson, professeur à l’ETH, qui a déjà
recherche sur les microrobots depuis des décennies. Le professeur Salvador Pané,
chimiste à l’Institut de robotique et de systèmes intelligents, et son équipe
ont développé des nanoparticules d’oxyde de fer parfaitement adaptées qui
un équilibre exigeant.
Un cathéter spécial libère une capsule contenant des médicaments
De plus, les microrobots contiennent également la substance active qu’ils transportent.
doivent être. Les chercheurs sont parvenus à combiner les microrobots avec des
médicaments pour différentes applications. Il s’agissait de
pour trouver un médicament qui dissout les thrombus, un antibiotique et un médicament contre les tumeurs.
médicament contre les tumeurs. Les médicaments sont libérés par un
un champ magnétique à haute fréquence qui chauffe les nanoparticules magnétiques et dissout ainsi l’enveloppe de gel et le microrobot.
Pour amener le microrobot à proximité de leur cible, les chercheurs ont utilisé des
chercheurs ont d’abord introduit un cathéter d’insertion. Le cathéter est doté d’un
Fil-guide relié à un préhenseur en polymère flexible.
Lorsque celui-ci est poussé au-delà du guide extérieur, il s’ouvre.
le préhenseur en polymère et libère le microrobot. Ensuite, le robot
Les chercheurs ont utilisé le microrobot magnétique via un système magnétique.
système de navigation au bon endroit.
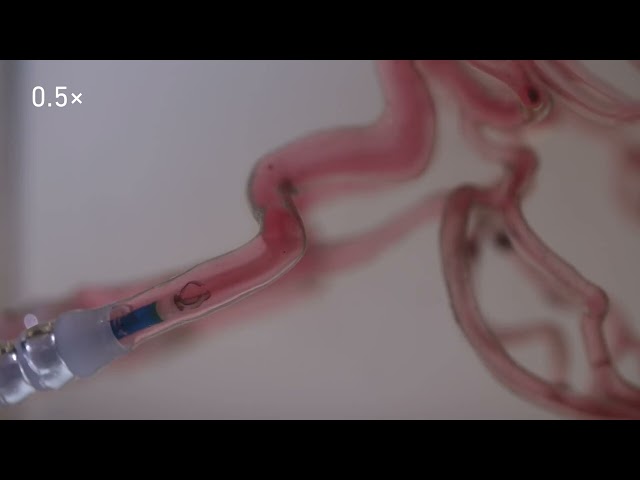
Ein handelsüblicher Einführkatheter mit Greifarm gibt den Mikroroboter frei. (Video: ETH Zürich)
Afin de pouvoir piloter les microrobots avec précision, les chercheurs ont développé un système de navigation électromagnétique modulaire adapté à une utilisation en salle d’opération. « Les vitesses du sang dans le système artériel humain varient fortement en fonction de l’emplacement. Cela rend la navigation d’un microrobot très complexe », explique Nelson. Les chercheurs ont combiné trois stratégies de navigation magnétique différentes, qui leur permettent de naviguer dans toutes les régions des artères de la tête.
Ils peuvent ainsi faire rouler la capsule le long de la paroi du vaisseau en utilisant un champ magnétique rotatif. La capsule peut ainsi être guidée très précisément vers sa destination à une vitesse de 4 millimètres par seconde.
Dans une autre variante, la capsule est déplacée avec un gradient de champ magnétique : le champ magnétique est plus fort à un endroit qu’à un autre. Le microrobot est ainsi attiré dans le récipient en direction du champ le plus fort. La capsule peut ainsi nager à contre-courant – et ce à une vitesse d’écoulement considérable de plus de 20 centimètres par seconde « C’est incroyable la quantité de sang qui est pompée dans nos vaisseaux et à quelle vitesse. Notre système de navigation doit être capable de supporter tout cela », explique Landers.
Lorsque le microrobot arrive à une bifurcation des vaisseaux, à travers laquelle il serait difficile de le manœuvrer, la navigation in-flow entre en jeu. Dans ce cas, le champ magnétique est appliqué à la paroi du vaisseau de telle sorte que la capsule est entraînée dans le bon vaisseau.

En combinant les trois variantes de navigation, les chercheurs sont parvenus à un contrôle robuste des microrobots dans une multitude de conditions d’écoulement et de scénarios anatomiques. Dans plus de 95% des cas testés, la capsule a délivré avec succès le médicament au bon endroit. « Les champs magnétiques conviennent parfaitement aux interventions mini-invasives, car ils pénètrent profondément dans le corps et – dans les intensités et les fréquences que nous utilisons – n’ont aucune influence sur le corps », explique Nelson.
L’innovation ne s’est pas arrêtée au robot
Afin de pouvoir tester les microrobots et leur navigation dans un environnement réaliste, les chercheurs ont développé des modèles en silicone dans lesquels ils ont reproduit exactement les vaisseaux sanguins des patients et des animaux. Ces modèles de vaisseaux sont si réalistes qu’ils sont désormais utilisés dans la formation des médecins et commercialisés par le spin-off de l’ETH Swiss Vascular. « Si ces modèles sont si importants pour nous, c’est parce que nous avons dû nous entraîner très souvent pour optimiser la stratégie et tous les composants. Cela ne peut pas se faire sur des animaux », explique Pané. Dans le modèle, les chercheurs ont pu dissoudre un caillot de sang de manière ciblée.

Mikroroboter löst Thrombus vollständig auf. (Video: ETH Zürich)
Après de nombreux essais réussis dans le modèle, l’équipe a également voulu prouver ce que le microrobot pouvait faire dans des conditions cliniques réelles. D’une part, ils ont pu montrer chez des porcs que les trois méthodes de navigation fonctionnent et que le microrobot reste bien visible pendant toute l’intervention. D’autre part, ils ont réussi à faire naviguer des microrobots à travers le liquide céphalorachidien chez un mouton. Landers s’en réjouit particulièrement : « Cet environnement anatomique complexe a un très grand potentiel pour d’autres interventions thérapeutiques, c’est pourquoi il était si excitant pour nous que le microrobot trouve également sa voie ici ».
Pas seulement utilisable pour les fermetures de récipients
Les nouveaux microrobots pourraient être utilisés non seulement en cas de thromboses, mais aussi en cas d’infections ou de tumeurs localisées. L’équipe de recherche a tenu compte, à chaque étape du développement, du fait que tout ce qu’ils mettent au point pourra être utilisé le plus rapidement possible en salle d’opération. Le prochain objectif est de commencer le plus rapidement possible les tests cliniques chez l’homme. Fabian Landers parle de la motivation qui s’empare de toute l’équipe : « A l’hôpital, les médecins font déjà un travail incroyable. Le fait d’avoir entre les mains une technologie qui nous permet d’aider plus rapidement et plus efficacement, et de redonner de l’espoir aux patients grâce à des thérapies inédites, nous motive ».
